Aumento de pecho en Valencia y Gandía
El aumento de pecho es una de las cirugías estéticas más demandadas tanto en nuestra clínica de Valencia como en la clínica del Dr, Moltó en Gandía. Este procedimiento no solo mejora la apariencia física, sino que también puede aumentar la confianza y la autoestima de las pacientes. A continuación, exploraremos los aspectos clave del aumento de pecho, incluyendo las técnicas utilizadas, los beneficios, el proceso de recuperación, y cómo elegir al cirujano adecuado.
Escucha el consejo del Dr. Moltó
¿Qué es el aumento de pecho?
El aumento de pecho, también conocido como mamoplastia de aumento, es una cirugía que tiene como objetivo aumentar el tamaño y mejorar la forma de los senos utilizando implantes mamarios. Este procedimiento es ideal para mujeres que desean aumentar el volumen de sus senos, corregir asimetrías o recuperar la forma y firmeza perdida tras el embarazo, la lactancia o la pérdida de peso.
Técnicas de aumento de pecho
- La más frecuente es recurrir a los implantes mamarios, de los que existe una amplia gama de posibilidades como verás más adelante.
- Otra forma es el aumento de pecho sin implantes con la propia grasa de la paciente. También llamado lipoestructura o lipofilling de senos y que tiene la ventaja de que en la misma cirugía plástica, se realiza una liposucción para extraer la grasa de una zona donde tienes exceso de ella. De este modo matamos 2 pájaros de un tiro, aumentamos el pecho y hacemos una liposucción en la misma cirugía.
- Otra opción es el aumento de pecho combinado con implantes y grasa propia.
Ejemplos de antes y después de aumento de pecho
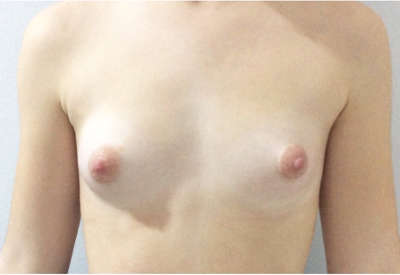
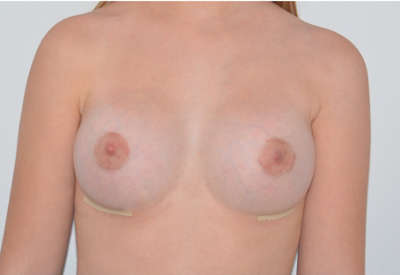
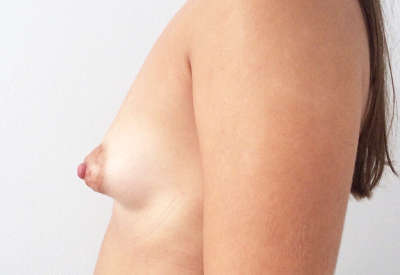
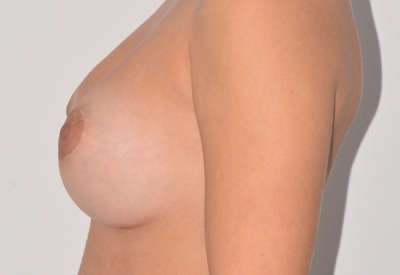
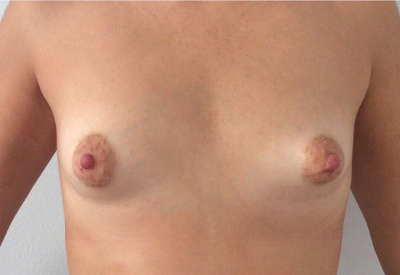
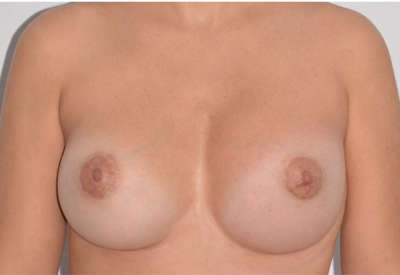
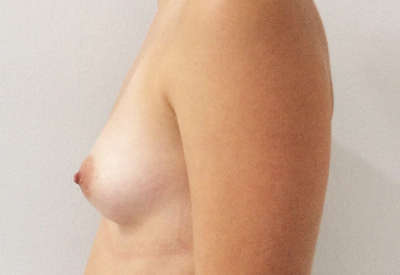

¿Quieres más información?
Completa el formulario y resolvemos todas tus dudas
Beneficios del aumento de pecho
- Mejora estética: Unos senos más voluminosos y bien formados pueden mejorar la proporción y armonía del cuerpo.
- Aumento de la confianza: Muchas mujeres reportan un aumento significativo en su autoestima y confianza tras la cirugía.
- Corrección de asimetrías: Los implantes pueden corregir diferencias en el tamaño o la forma de los senos.
Proceso de recuperación
El proceso de recuperación varía según la técnica utilizada y la anatomía individual de la paciente. Generalmente, se recomienda reposo durante las primeras 48 horas y evitar actividades físicas intensas durante al menos cuatro semanas. Es crucial seguir todas las indicaciones del cirujano para asegurar una recuperación rápida y sin complicaciones.
Elección del cirujano adecuado. Aumento de pecho en Valencia y Gandía
¿Porqué el Dr. Moltó es la mejor opción como cirujano? Seleccionar un cirujano calificado y experimentado es fundamental para el éxito del aumento de pecho, ten en cuenta siempre:
- Credenciales y experiencia: EL Dr. Moltó es un cirujano altamente certificado y tiene una gran experiencia específica en mamoplastias de aumento.
- Opiniones y testimonios: Lee las opiniones de otras pacientes para obtener una idea de los resultados que puedes esperar.
- Consultas iniciales: Aprovecha las consultas iniciales para discutir tus expectativas y evaluar la comodidad y confianza con el cirujano.
Aumento de pecho en Valencia
Valencia, con su amplia oferta de clínicas especializadas y cirujanos expertos, es un destino ideal para someterse a una mamoplastia de aumento. Entre estos profesionales destaca el Dr. Moltó, quien ofrece tecnología avanzada y un entorno cómodo para la recuperación. Su experiencia y reputación en la cirugía estética garantizan resultados óptimos para sus pacientes.
Aumento de pecho en Gandía
Gandía, aunque más pequeña que Valencia, cuenta con el Dr. Moltó como un referente en cirugía estética. La tranquilidad y belleza de esta ciudad costera, junto con la profesionalidad del Dr. Moltó, proporcionan un entorno relajante y seguro para tu recuperación. Para más información, visita Dr. Moltó.
¿Por qué hacer tu aumento en clínicas Dr. Moltó?
- Especialista en cirugía estética de pechos con +30 años de experiencia.
- Prótesis mentor: las mejores del mercado.
- Revisiones con ecografía incluída.
- Financiación hasta 24 meses sin intereses y máximo hasta 5 años.
- Hospital IMED: tecnología puntera y lujo. Habitación individual.
El aumento de pecho es una opción excelente para mejorar la apariencia y autoestima de las mujeres. Con las técnicas avanzadas disponibles en Valencia y Gandía, las pacientes pueden esperar resultados naturales y satisfactorios. Si estás considerando esta cirugía, asegúrate de investigar bien y elegir un cirujano con experiencia y buenas referencias.
¿Quieres más información sobre el aumento de pecho en Valencia y Gandía?
Completa el formulario y resolvemos todas tus dudas
Tipos de prótesis mamarias
Material y Recubrimiento
Las prótesis mamarias actuales están recubiertas de silicona, que puede ser rugosa o lisa.
Tipos de relleno
- Suero Salino: Más económico, permite ajustes de tamaño.
- Gel de Silicona Cohesivo: Ofrece un aspecto y tacto más natural.
Innovación: Prótesis B-Lite
- Ligereza: Hasta un 30% más ligeras que otras de silicona.
- Recomendación: Ideal para aumentos grandes (a partir de 400 cc).
Formas de prótesis
- Prótesis redondas: Aumentan la forma existente del pecho, ideal para pechos pequeños con buena forma.
- Prótesis anatómicas: Adecuadas para pechos con formas anómalas (tubulares o ptosicos), más costosas, pero ofrecen una apariencia natural donde se necesita.
Selección de implantes
La selección entre redondas y anatómicas depende de la forma inicial del pecho y el resultado deseado. Implantes anatómicos no son siempre necesarios y pueden añadir un coste adicional de unos 500 euros sin aportar ventajas significativas en todos los casos.
¿Quieres más información sobre el aumento de pecho en Valencia y Gandía?
Completa el formulario y resolvemos todas tus dudas
Colocación de implantes mamarios
Ubicaciones de los Implantes
- Subfascial: Implante bajo la membrana que envuelve el músculo pectoral. Es ideal para implantes moderados o anatómicos con un buen “pinch” (grosor del tejido >1.5 cm). Limitado por menor cobertura del implante comparado con la submuscular.
- Submuscular: Ubicación debajo del músculo pectoral. Es la opción más común y recomendada debido a que ofrece un resultado más natural, especialmente en la parte superior del pecho y el escote. Aunque el postoperatorio es más molesto, vale la pena por los resultados satisfactorios.
- Subglandular: Colocación debajo de la glándula mamaria. Tiene inconvenientes como el contacto directo de la prótesis con la glándula, lo que puede llevar a contaminación y resultados menos naturales. No se recomienda generalmente – Si te la ofrecen di: no gracias..
Consideraciones técnicas
- Subfascial: Buen “pinch” (>1.5 cm) necesario. Menor cobertura del implante.
- Submuscular: Cobertura del músculo, mejor para implantes moderados y grandes. Postoperatorio más doloroso pero resultados óptimos.
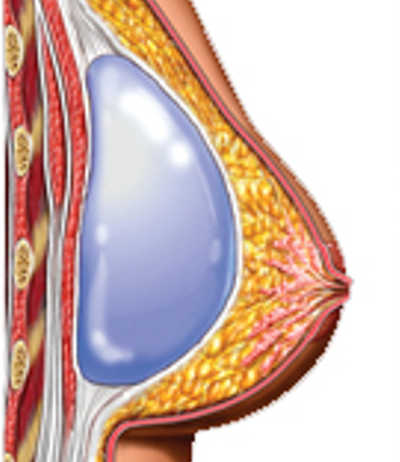
subfascial
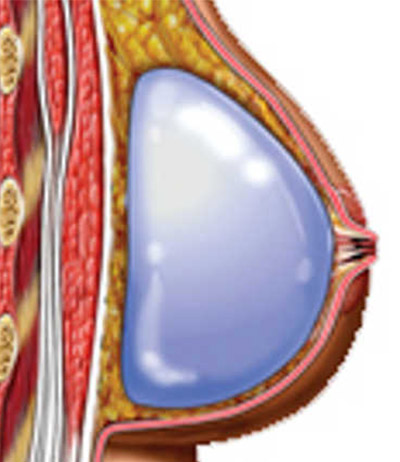
submuscular
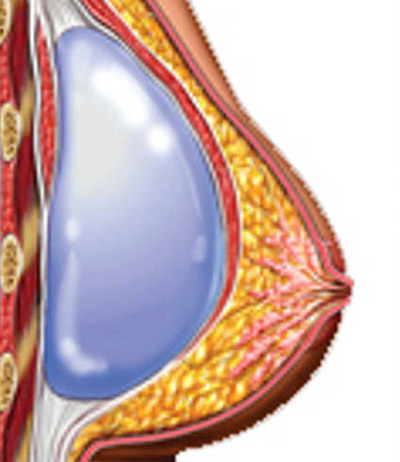
submuscular
¿Quieres más información?
Completa el formulario y resolvemos todas tus dudas
¿Qué opinan nuestros pacientes?
Preguntas frecuentes
¿Cuánto cuesta una cirugía de aumento de pecho?
El costo puede variar dependiendo de varios factores, incluyendo el tipo de implante y la clínica. En Valencia y Gandía, los precios pueden oscilar entre 4,000 y 7,000 euros.
¿Cuáles son los riesgos asociados?
Como cualquier cirugía, el aumento de pecho conlleva riesgos, como infecciones, sangrado, y complicaciones relacionadas con los implantes. Es esencial discutir estos riesgos con tu cirujano.
¿Cuándo podré ver los resultados finales?
Aunque se notará un cambio inmediato, los resultados finales pueden apreciarse después de varios meses, cuando la inflamación haya disminuido completamente.
¿Quién es una buena candidata para el aumento de pecho?
Esta cirugía plástica tiene pocos requisitos y contraindicaciones.
Básicamente cualquier mujer que desee un cambio que quiera encontrarse más a gusto con su físico.
Si estás pensando en aumentar tu pecho, el doctor Moltó generalmente te va a pedir:
- Que tengas un estado de salud razonablemente bueno.
- Que hayas finalizado tu periodo de crecimiento.
- Que tus expectativas sean realistas.
- Que la forma o el tamaño de tu pecho te cause un trastorno.
El aumento del pecho es una cirugía plástica y como tal es muy personal. No la debes realizar para nadie y tampoco solo al gusto de alguien.
¿Cómo son las consultas preoperatorias para tu mamoplastia de aumento con el Dr. Moltó?
Tendremos varias consultas o citas antes de la intervención.
En la primera consulta:
- Evaluaremos tu historial médico: miraremos tu estado de salud de una forma muy genérica, antecedentes médicos e historial familiar, hábitos como fumar , cirugías previas…
- Exploración física: tenemos que ver el tamaño y la forma de tu pecho actual. Esta exploración nos servirá para recomendarte un volumen preferible para tu aumento.
- Objetivos quirúrgicos: saber cuales son tus ideas de aumento, qué resultado final buscas.
- Si es útil para tu caso, te realizaremos una ECOGRAFIA para valorar mejor la situación, esta ecografía la realizamos nosotros en la consulta y va incluida en tu presupuesto, por lo que no te supondrá ningún gasto extra.
- Te daremos los consentimientos informados para que puedas acceder a toda la información en cuanto a posibles riesgos o complicaciones.
- Te facilitaremos un presupuesto personalizado, te informaremos sobre formas de pago, financiación…
«El Dr. Moltó tee recomendará el tipo de implante, la vía de abordaje (por donde lo vamos a colocar) y el tipo de colocación, además de los cuidados postoperatorios que deberás llevar.»
En una segunda entrevista también directamente con el Dr. Moltó, en la que revisaremos los puntos anteriores uno por uno y aclararemos cualquier posible duda o inquietud que te haya podido surgir.
2ª visita con el dr. Moltó
En el momento lo desees, una vez te hayas decidido puedes pedir esta segunda entrevista, en ella repasaremos lo anterior y resolveremos las posibles dudas.
Una vez tomada la decisión fijaremos la fecha de la cirugía de aumento de mamas y te solicitaremos un estudio preoperatorio o veremos los resultados en caso de que lo traigas ya
Características de la intervención de la cirugía de aumento de pecho
- Antes de la cirugía el Dr Moltó te realizará el diseño prequirúrgico, que son las medidas que tomamos y marcas que realizamos en la piel con un rotulador para que sirvan de guía en la cirugía.
- En la mayoría de los casos se realiza con anestesia general, por lo que estarás totalmente dormida durante toda la intervención.
- La duración de la cirugía suele der de entre 1 y 2 horas.
- Tras un periodo de reposo en el área de recuperación (despertar) cuando el anestesista compruebe que estás perfectamente bien, te llevarán a la habitación para que descanses.
- Más tarde, el Dr Moltó pasará por tu habitación para comprobar que te encuentras perfectamente y que no tienes dudas. En esos momentos te explicaremos como ha ido la cirugía y el resultado final de la misma.
- Hospitalización durante 1 noche en el hospital IMED en habitación individual.
¿Cómo es el alta después de la intervención de la cirugía de aumento de pecho?
En la mayoría de los casos, al día siguiente por la mañana el Dr Moltó o un médico de su equipo, pasará a verte.
Comprobaremos que estás bien, te hacemos la cura cambiando el vendaje por el sujetador deportivo y te entregamos un informe de alta con nuestras instrucciones:
- La medicación que debes de tomar.
- La fecha de la próxima cita.
- Un teléfono en el que algún medico del equipo estará disponible las 24 horas del día para que le puedas consultar cualquier duda.
Si tienes cualquier duda sobre como debe de ser tu día a día después de tu aumento de senos, contáctanos.
¿Cuál es el Precio de aumento de pecho en Valencia y Gandía con el Dr. Moltó?
El precio de una operación de aumento de pecho con prótesis viene determinado por la suma de gran cantidad de factores entre los que se encuentran:
- los honorarios del médico anestesista,
- el alquiler de quirófanos del hospital,
- las pruebas médicas que sean necesarias en tu caso,
- el tipo de prótesis que elijas para la intervención,
- los honorarios del cirujano,
- tiempo de hospitalización,
- el material quirúrgico, las prendas de post-cirugía, las recetas para los medicamentos del postoperatorio y la recuperación, las visitas de seguimiento, …
Cuando tu como paciente nos preguntas por el precio de un aumento de pecho con prótesis, debes de tener en cuenta que para nosotros, lo más importante es tu salud.
En nuestra clínica solo utilizamos las mejores prótesis del mercado (Allergan).
En cualquier caso el precio depende de las características fisicas y de las elecciones personales de cada paciente.
¿Cuánto pecho me pongo?
Una de las decisiones que más inquieta a las pacientes que se van a realizar un implante corresponde a las del volumen de sus futuros pechos, es decir “cuánto me pongo”
“Te puedes poner un implante todo lo grande que admita tu anatomía.”
No creas que hay tanto margen de variación, el implante que seleccionemos deberá tener de base exactamente de lo que mida la mitad de tu tórax de ancho.
De esta forma nos aseguramos que rellene desde la zona central (el famoso canalillo).
- Si escogiéramos un implante pequeño, la parte central puede quedar vacía.
- Por el contrario si escogemos uno demasiado grande podría no caber y que la prótesis quede formando pliegues (Rippling de pecho), que se palparán y serán visibles en algunos casos al no poder expandirse adecuadamente.
Nosotros te mediremos detenidamente y escucharemos tus deseos de cambio ya que cada paciente tiene un gusto diferente.
“Independientemente de nuestra recomendación del tamaño del implante, cada paciente elige el tipo de pecho que quiere tener.”
¿Influye la forma del pecho en el resultado final?
Si las mamas no son completamente simétricas antes de la cirugía, es difícil que lo sean después.
Si existe alguna asimetría siempre se mejora, pero es probable que parte de esa diferencia entre ambos pechos permanezca.
“Cuanto más simétrico sea el pecho en el preoperatorio más simétrico será después.”
¿Se tienen que cambiar las prótesis cada 10 años?
Rotundamente NO.
Todas las prótesis presentan una tasa de rotura que en la marca MENTOR que es la única que nosotros implantamos, está alrededor del 2% a los diez años.
Es la tasa más baja que ofrecen las diferentes marcas de implantes hoy en día.
Si las prótesis son de buena calidad como es el caso de las que el doctor Moltó utiliza, no deberás cambiarlas a no ser que éstas se rompan.
¿Cuánto tardaré en poder hacer deporte?
Durante las dos primeras semanas debes guardar reposo deportivo.
A partir de ahí puedes realizar ejercicio de forma moderada que no implique los músculos pectorales, lo que en lenguaje técnico se llama “tren superior”.
Básicamente debes excluir de tu práctica deportiva durante las primeras 6 a 8 semanas deportes como pádel, tenis, natación, submarinismo, golf, escalada… y spinning si te levantas mucho de la bicicleta.
Ejercicios de alta intensidad como levantamiento de pesas o el crossfit tras el aumento de pecho o mastopexia u otra cirugía de aumento mamario, deben de pausarse durante este período y es muy recomendable pedir consejo al Dr. Moltó antes de reiniciar su práctica
¿Qué edad es buena para un aumento de pecho?
Cualquier edad es buena a partir de cierto grado de madurez, tanto física como mental.
Nosotros no recomendamos la cirugía hasta alcanzados los 18 años, debido a que hasta esa edad la forma de las mamas puede variar, lo que impedirá planificar la cirugía adecuadamente.
¿Qué deportes puedo practicar llevando implantes?
La posibilidad de practicar deportes con prótesis de mama son las mismas que si no las llevaras.
Únicamente si los implantes son grandes o subfasciales deberás usar ropa deportiva adecuada para obtener una buena sujeción.
Nosotros, para que el resultado estético dure lo máximo, te vamos a recomendar que no realices ejercicios de la zona pectoral del tipo musculación. Un pectoral demasiado potente comprimirá las prótesis con mucha energía, y puede hacer que el bolsillo en el que estas están alojadas se haga un poco más grande de lo normal, afectando al resultado estético.
Por tanto trabajar los pectorales, si las llevas submusculares no es la mejor idea.
Ten en cuenta que el músculo está encima del implante y por lo tanto cada vez que se contraiga lo deformará.
Si la colocación es subfascial no hay ningún problema mientras lleves una sujeción del pecho adecuado.